卡利奇霉素γ1(Calicheamicin γ1)所代表的 1,5- 二炔 -3- 烯(enediyne)类抗生素。有记录一个分子足以杀死一个细菌:
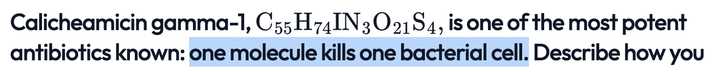
它的结构堪称自然演化出的化学武器的极致,无论从超规格毒性,作用机制,还是分子的复杂性,都体现了自然演化的暴力美学。
其结构分三个部分:三硫键触发器(红框),杀伤性的烯二炔(蓝圈)和余下的用于精准制导的四糖单元(包含特殊的羟胺类 N-O 糖苷键,绿圈)。三个部分相辅相成,协同作用,精确锁定敌方的 DNA,将其一刀两断,相当于在万军丛中直取敌方将领首级,令敌军群龙无首而溃败。
那么,假设你现在是《自然选择》项目组武器开发部的首席架构师,你是如何设计出如此精巧的化学武器的?
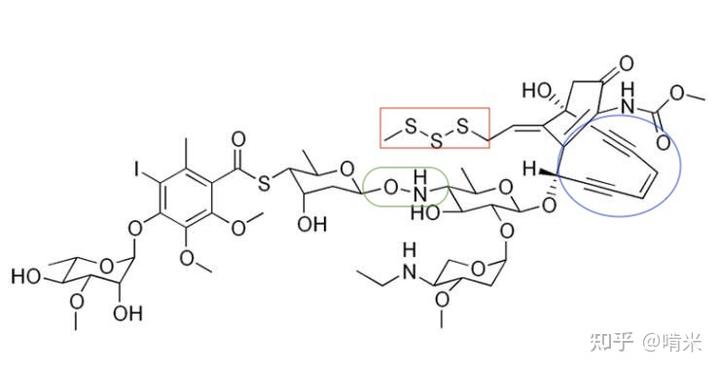
彼时,微生物界的内卷已到了白热化阶段。在有限的泥土里抢营养,常规的武器比如β- 内酰胺和大环内酯,靠的是攻破城池(细胞壁)和打击军工厂(抑制翻译),太慢了。而且,对手项目组很快就能写出抗性基因(比如 β- 内酰胺酶)来反制。
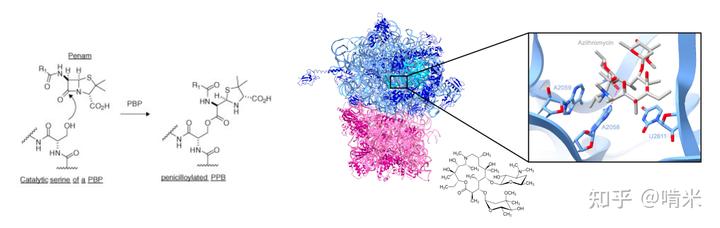
因此,你司需要开发一种更致命的武器,不搞代谢干扰,直接摧毁敌方的源代码(DNA),最好一击必杀,只要一两个分子命中,就能让对手盘的细胞们当场宕机和凋亡。
要切断 DNA 双螺旋的稳定骨架,所需的能量极大,常规的化学手段难以做到,你需要活性极高的自由基,并且要到敌方大本营后再产生,不然自己就先被炸死了。因此,这种自由基的产生必须依赖某种极强的化学驱动力,在合适的位点和精密的触发条件下,被驱动引爆。
芳香化,就是这个极强的驱动力,电子得以离域,产生苯环这类极度稳定的结构,并释放大量能量。
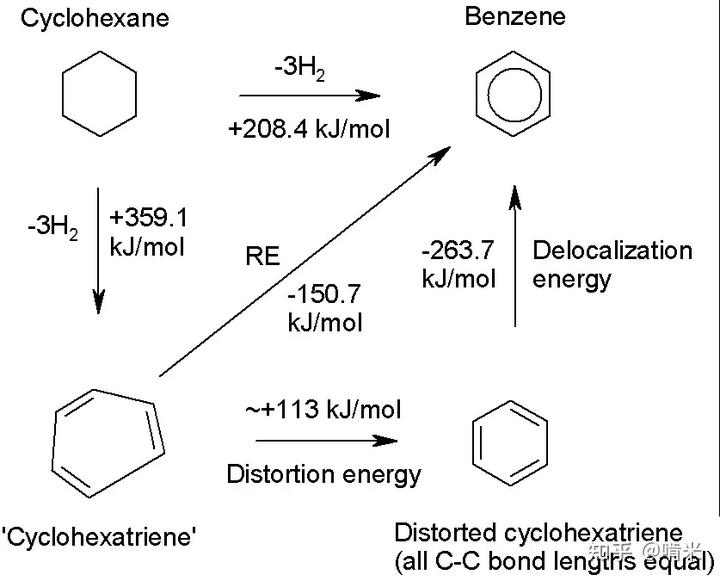
当把两个炔基中间夹一个烯基组合起来(烯二炔),只要给这个体系一点点能量,或者改变一下构象,让两端的炔基向中间靠拢,距离小于 3.2Å时,旧键断裂,新键生成,分子瞬间向内塌缩成一个1,4- 去氢苯的双自由基。
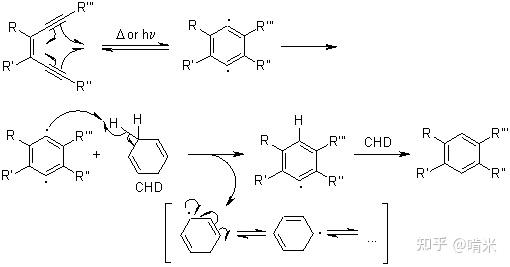
这个双自由基必须立刻从周围随便什么东西身上抢走两个氢原子来填补自己,形成稳定的苯环。如果它刚好以一个特殊的姿势贴在 DNA 上,它就能毫不留情地在几乎同一时间把 DNA 两条链上的氢原子硬生生各扯下来一个(一个去抢某条链的 C5' 上的氢,另一个去抢互补链 C4' 上的氢),自由基转移到 DNA 上后,会启动一系列氧化降解反应,导致 DNA 双链断裂(DSB)。
假如是单链断裂(SSB),细胞还可以通过碱基切除修复(BER)和单链断裂修复(SSB repair)机制,准确修补缺口。但在位置相近且同时断裂的双链处(卡利奇霉素造成的断裂通常相隔 2-3 个碱基对),细胞无法获得修复模板,同源重组修复(HRR)或非同源末端连接(NHEJ)极易出错,如果断裂发生在关键的基因(比如管家基因),那么细胞面临的结局就只剩周期停滞或凋亡。
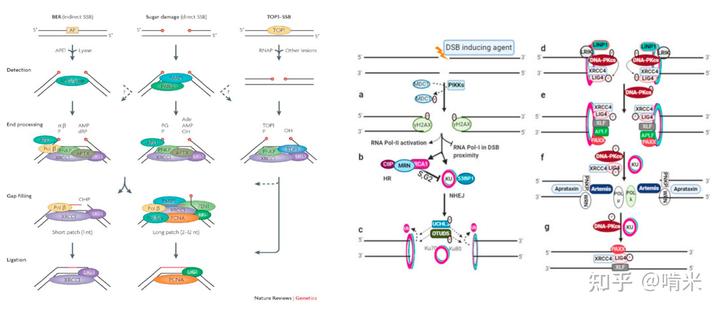
这种依靠双自由基同时产生,同时转移到 DNA 的两条链上,在极近的位置,在修复工程没有反应过来的刹那间,以唯快不破之势切断双链,便是“一分子杀一细胞”的化学基础。
那么接下里,就是亿些些工程学问题了:如何促发双自由基的产生?
首先必须得有环的刚性约束,不然两个炔基太自由,甩来甩去迟早爆炸。且环不能太小,小了张力大,俩炔基贴得近,容易擦枪走火,所以最后锁定在 9-11 元环。
如果把它做成 9 元环(比如新制癌菌素,NCS),张力还是有点大,绷得紧,放身上仍比较容易自己就炸了。做成 11 元环(比如 Uncialamycin),环松了,活化能高,扔进敌方阵地,也可能只是个闷炮。
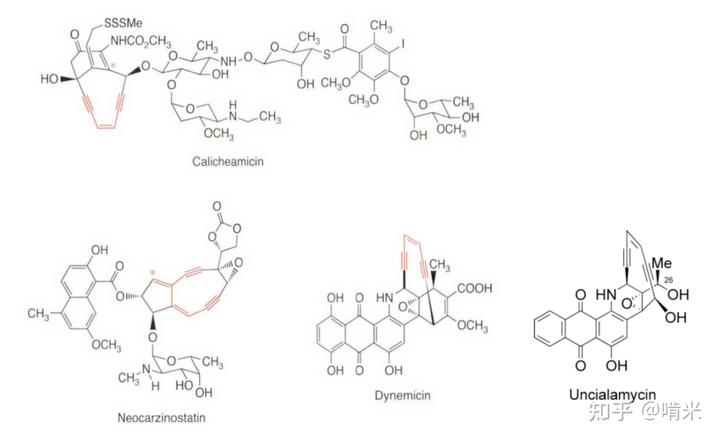
卡利奇霉素的 10 元环,环张力刚刚好。在正常状态下,两个炔基的距离大约是 3.3-3.6 埃,够不太着,非常稳定。你只需再设计一个巧妙的“扳机”,在它到达敌方阵地时,稍微推一把,把距离缩短到 3.2 埃以内,就能起爆产生双自由基。
为了造这个扳机,你给烯二炔体系配上了一个甲基三硫化物(-SSSCH3)基团。为什么是它?因为细胞外的环境(血液、泥土)是氧化性的,即便胞外有水,氨基这样的亲核基团,它们都太“硬”了无法扣动这个扳机,能扣动这个基团的必须是个“软”亲核体,比如巯基(-SH,-2 价),但在氧化氛围下,游离巯基很难存在,大多形成双硫键(-SS-,-1 价)被藏了起来。
在细胞内部,特别是增殖旺盛的肿瘤细胞或竞争细菌内部,为了抵抗氧化应激,这些细胞疯狂燃烧能量维持电子链的传递,驱动谷胱甘肽还原酶,强行把 GSSG 劈开,维持高浓度的单体谷胱甘肽(GSH)。
所以,当卡利奇霉素游荡在胞外时,三硫化物没啥反应,炸弹处于保险状态。一旦分子穿透细胞膜,进入敌方内部,高浓度的 GSH 就是扣动扳机的手指:GSH 亲核进攻三硫化物的 S-S 键,释放出一个极其活泼的硫醇,接着这个硫醇通过分子内 Michael 加成,攻击分子内相邻的α,β- 不饱和酮,导致桥头碳原子从 sp²杂化变成了 sp³杂化,环的构象突变,通过机械的杠杆传动,迫使两个炔基靠近,从不反应的 3.6 埃,弯曲成一点就着的 3.0 埃。
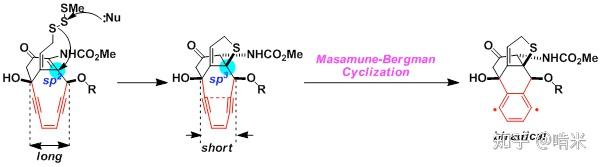
炸弹有了,扳机有了,现在需要的是制导系统。你不能让双自由基在细胞质里瞎炸,必须把它精确地定位在敌方 DNA 上。
于是,你给弹头配上了一条长长的芳基四糖链,这条糖链没有普通糖类大量亲水的羟基,而且为了增加脂溶性,方便挤进 DNA 小沟(Minor Groove),带上了甲氨基和各种奇怪的修饰。生理环境下,带正电的氨基刚好和 DNA 骨架上带负电的磷酸盐形成盐桥,再通过多重非共价相互作用,使分子就像一个量身定制的卡钳,能严丝合缝地卡进 DNA 的 5'-TCCT-3' 序列,锚定在发射位置上。
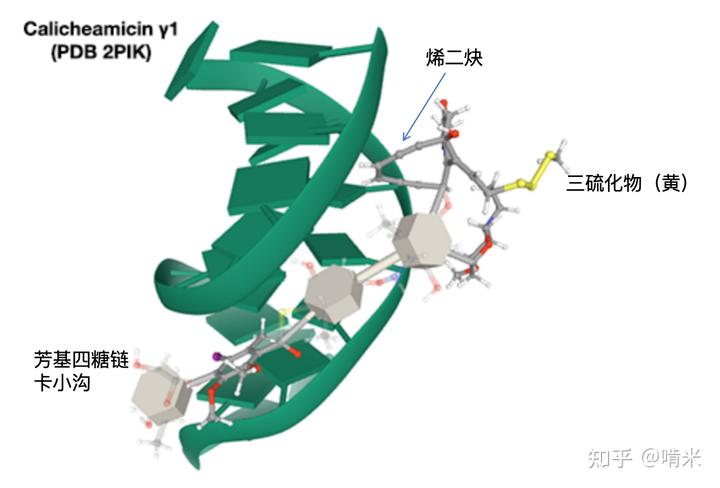
如此一来,你的分子就像一只毒蝎一样,完美地潜伏在敌方 DNA 的关键命门,现在只需利用敌方本身的高 GSH 的代谢特征,静静等待一个不长眼的 GSH 扣动扳机,将毒刺扎进 DNA 完成刺杀任务就行了。
至于那个特殊的羟胺类 N-O 糖苷键,是你埋在这个制导系统里的一道保险栓,当环境威胁解除,留着这么多高毒的弹药对自己也是个威胁,所以用这个特殊的 N-O 键作为后门,方便拆卸,剩下的裸弹头由于失去了锚定 DNA 的能力,其毒性会断崖式下降 。为了节省能量,负责拆卸和组装的酶是同一套糖苷转移酶(CalG)(反应可逆),如此也符合原子经济性,战时能快速调配组装出武器。
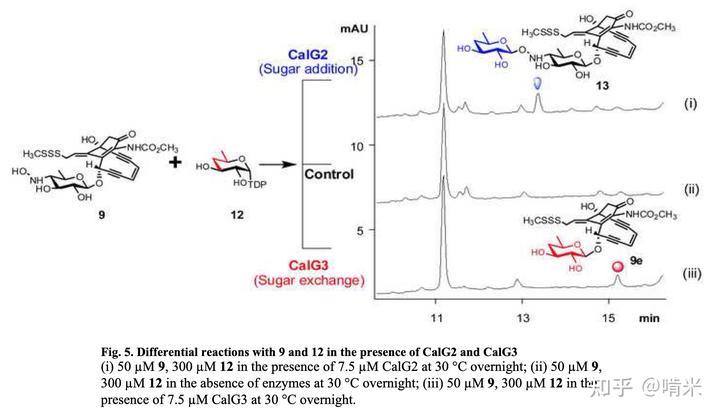
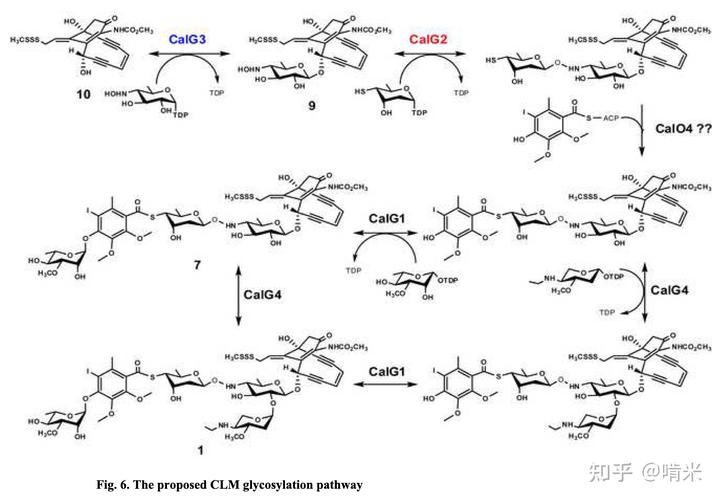
显然,仅有这一道保险栓是不够的,卸载糖基只是瓦解了识别 DNA 的能力,烯二炔这个火药桶仍是易燃易爆。为了防止被自己造的炸药炸死,你需要更多的保险措施。
比较得体的方式是收刀入鞘:对于那些环张力极大的,容易擦枪走火的 9 元环(NCS)和某些 10 元环(天慈霉素,TNM),你编码了一种桶状结构的抗性蛋白(TnmS),这个蛋白具有皮摩尔级的超高亲和力,它像蚌壳一样,把烯二炔基团死死包裹在疏水内腔里,锁死烯二炔的构象,让它无法弯曲产生 Bergman 环化,当需要把炸弹扔出去时,蛋白壳才打开释放武器。
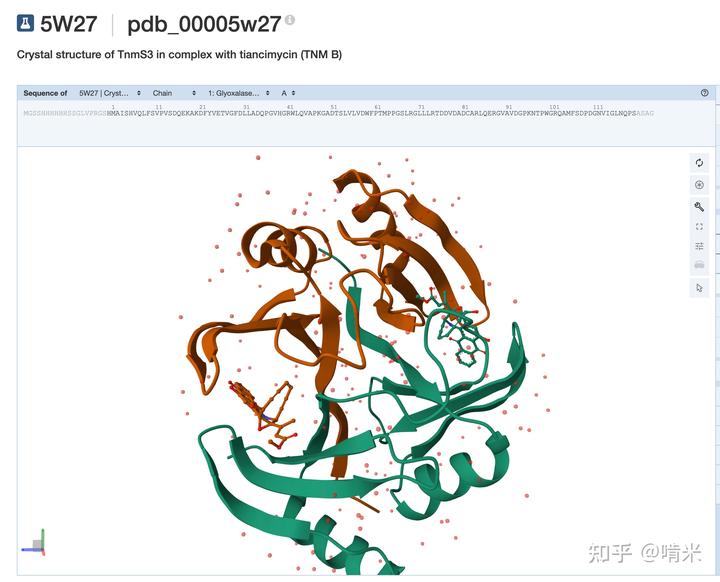
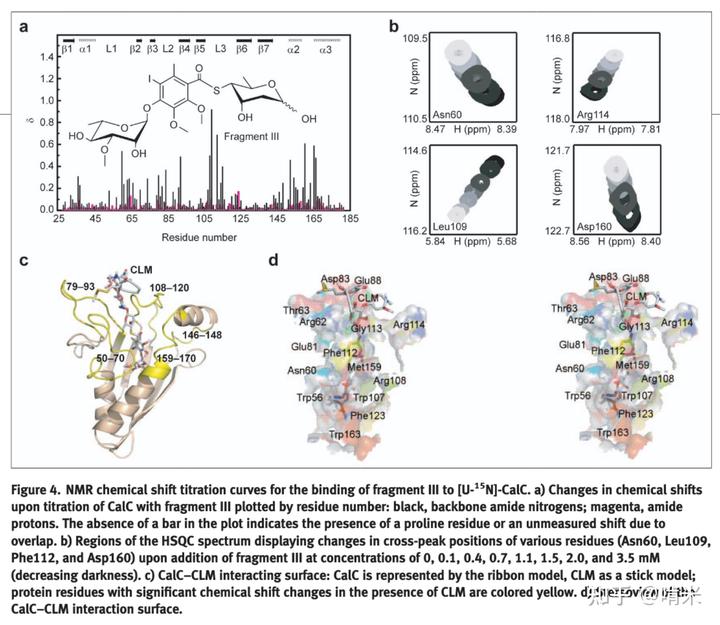
对于卡利奇霉素这种采用三硫化物扳机的 10 元环,万一细胞内 GSH 浓度波动导致走火怎么办?你设计了一个名为 CalC 的蛋白用于一换一。
CalC 把炸弹抱在怀里随时准备牺牲自己,它通过芳基四糖抓住卡利奇霉素,同时三硫化物扳机暴露在胞质中,假如被意外激活,自由基产生位点正好对着 CalC 的 Gly113 的 Cα- 氢原子,能被瞬间中和。结果是卡利奇霉素和 CalC 都成了次抛,它们的残骸只能被分解,无法二次利用,补充弹药库时两者都需从头合成,而合成卡利奇霉素涉及几十种酶,所以这个方式是非常惨烈和浪费的。
当然,还有一种更简洁高效但非常不体面的方式,直接外排毒素,死道友不死贫道,爱咋咋地,我能好好活着就行。
纵使“一分子杀一细胞”的杀手未来层出不穷,比如蓖麻毒素的 A 链分子,能精确切除 28S 核糖体 RNA 上的一个腺嘌呤,致使细胞内的核糖体一个个失活,最终关闭该细胞的所有蛋白质合成而 go die;白喉毒素A 亚基,有 ADP- 核糖基转移酶活性,靶向真核细胞的延长因子 EF-2 ,催化修饰后的 EF-2 丧失功能,无法参与核糖体转位,同样导致蛋白质合成完全中断;霍乱毒素,持续给 G 蛋白添加 ADP 分子,使其永久激活,直到整个细胞的信号系统紊乱而 go die;朊病毒,诱导序列完全一致的肽段错误折叠,指数级复制自己这套无生理活性又代谢不掉的空间排列“模因”,慢慢杀死一个个体……
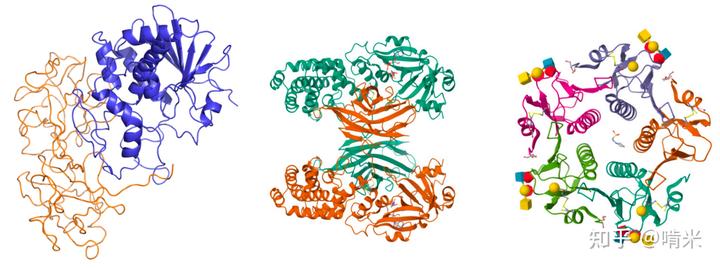
但以上这些杀手,基本都是间接作用和催化机制,有个猥琐发育的过程,没一个像烯二炔类抗生素那样直接了当,一击截断对手的遗传蓝图。并且,烯二炔类分子的体积是它们之间最小的,其他全是大分子蛋白,烯二炔以小搏大,可见其携带的杀伤信息密度是极高的。
这套毁灭系统过于成功,以至于吸引了后世智人的注目,他们在这套系统上又整了个“生物洲际导弹”——抗体。抗体 - 药物偶联物(ADC)的抗体部分负责在茫茫细胞中识别特定靶标,将药物精准投送至特定的肿瘤细胞表面;内吞进细胞后,连接子裂解释放烯二炔毒素;四糖基接管精准制导系统,识别 DNA;肿瘤细胞自身的 GSH 亲手扣动扳机;双自由基瞬间掐断 DNA。一套组合拳下来,精准地将肿瘤细胞杀死而无伤正常细胞。
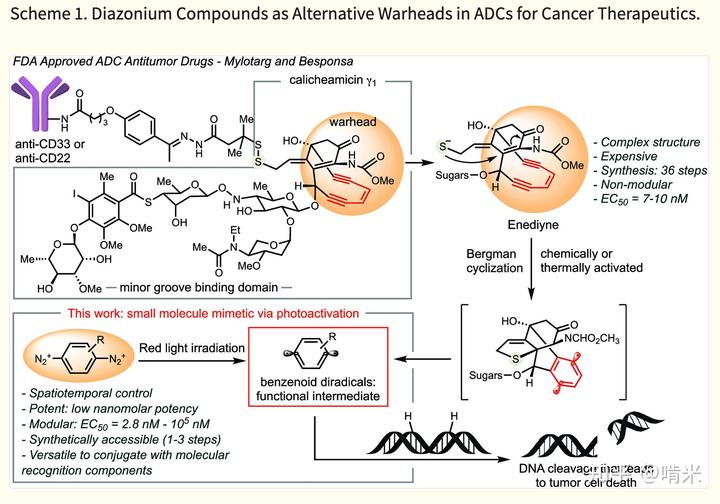
两款装载烯二炔(卡里奇霉素 payload)的 ADC 药物 Mylotarg(吉妥珠单抗奥佐米星)和 Besponsa(贝斯利珠单抗奥佐米星)已上市,用于治疗急性骨髓性白血病和淋巴细胞白血病。值得一提的是,吉妥珠单抗于 2000 年 5 月获批上市,是首款上市的 ADC,比第二款 ADC 药物 Adcetris(维布妥昔单抗,靶向 CD30)早了整整 11 年,足见 Pfizer 远超时代的预见性。
而新一代以环张力更小的 Uncialamycin 为载荷的烯二炔类 ADC 也正冉冉升起,毕竟只要抗体带路到肿瘤细胞,切不切 DNA 并不是最重要的,在里面嘎嘎乱杀弄死肿瘤细胞就行,所以四糖单元并不是必需的。如此一来,合成也能简单很多,少了糖环和 N-O 键,又扩成 11 元环,化合物稳定性也得到了显著提升。
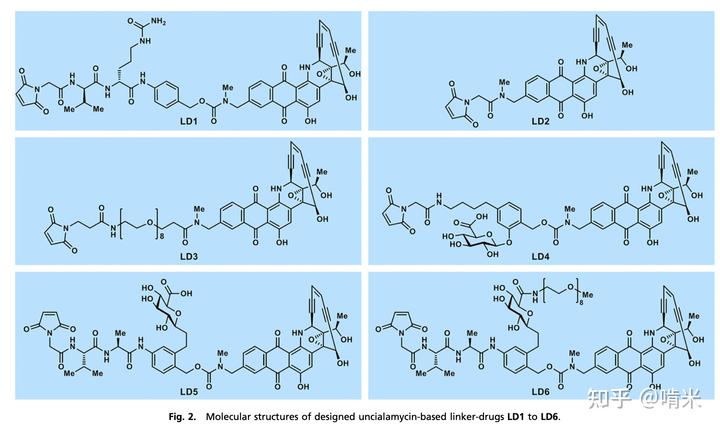
从毒到药,烯二炔的故事仍在进行中,远没有完结。
但武器开发部架构师的体验到此告一段落,不过瘾的可以看看我的其他作品:
