【2021.7.28 更新】
好多人私信我问我有没有关于四氧化三铁晶体结构更新的图,这些图看上去都有些年头了。的确这份文献是我读大学二年级的时候,从学校的纸质版期刊中影印下来,然后重新扫描成电子版的。
关于四氧化三铁反尖晶石结构更清晰的图,我这里也找了一个:
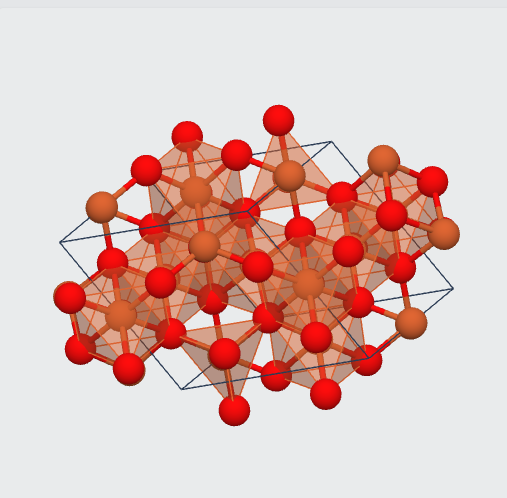
以及有关这幅图的解析[1]:
Fe3O4 is Spinel-derived structured and crystallizes in the trigonal R-3m space group. The structure is three-dimensional. there are three inequivalent Fe+2.67+ sites. In the first Fe+2.67+ site, Fe+2.67+ is bonded to six O2- atoms to form FeO6 octahedra that share corners with six equivalent FeO4 tetrahedra and edges with six FeO6 octahedra. There are two shorter (2.08 Å) and four longer (2.11 Å) Fe–O bond lengths. In the second Fe+2.67+ site, Fe+2.67+ is bonded to six equivalent O2- atoms to form FeO6 octahedra that share corners with six equivalent FeO4 tetrahedra and edges with six equivalent FeO6 octahedra. All Fe–O bond lengths are 2.06 Å. In the third Fe+2.67+ site, Fe+2.67+ is bonded to four O2- atoms to form corner-sharing FeO4 tetrahedra. The corner-sharing octahedra tilt angles range from 54–57°. All Fe–O bond lengths are 1.92 Å. There are two inequivalent O2- sites. In the first O2- site, O2- is bonded in a rectangular see-saw-like geometry to four Fe+2.67+ atoms. In the second O2- site, O2- is bonded in a distorted rectangular see-saw-like geometry to four Fe+2.67+ atoms
【2021.7.6 更新】
没想到把以前一个我很感兴趣所以查了一些文献的问题所收集的资料随手整理的一个回答,居然是收获了不少人的回音。有些私信也来问我一些问题,所以索性就补充一点东西吧。
首先说明,我的专业不是无机化学,只是因为不少诸如此类的问题从我开始学化学起就一直萦绕心头,囿于当时条件,直到读了大学才开始在图书馆中查各种资料,才能够慢慢得出结论。所以有些观点难免会有所失误,见笑大方。希望专业人士不吝赐教。
我提到【高中化学教材会把它简单理解成 Fe2O3.FeO】,这里涉及到 2 个问题:
(1)在计算题中,的确可以把 Fe3O4 看成 Fe2O3.FeO,就像计算的时候可以把葡萄糖 C6H12O6 当成 C6.(H2O)6 一样。
(2)在平时论述中,能否这样写,这个涉及到无机化学中很多物质写成氧化物的【形式】。
比如钠的硅酸盐经常写成
或者
,这样做的好处是可以方便了解其中的钠 - 硅比,钠 - 氧比和硅 - 氧比。现实世界远比卷面教材上复杂,实际上化学式严格符合 Na2SiO3 的硅酸钠是极度罕见的。因此都是根据实测结果判断,某一特定条件下制备出来的水玻璃其中元素比是多少,进而计算出其化学式。
这种写成氧化物形式的写法在矿物学中尤其用的多。因为矿石分析中,最后得到的数据都是元素组成和含量比关系。从这个角度说,四氧化三铁写成 Fe2O3.FeO,其实不能算完全错误,毕竟其中的确就是含有铁离子、亚铁离子以及氧离子。只是这种写法过于笼统,而且容易产生混淆。当然旧教材和某些落伍的莫名其妙的教辅书说是铁酸亚铁那就肯定是错的了。
四氧化三铁虽然和酸反应会生成铁盐和亚铁盐,所以很多高中化学教材会把它简单理解成 Fe2O3.FeO,但是四氧化三铁绝对不等于氧化铁和氧化亚铁的混合物。
过去曾经对四氧化三铁有诸多种写法:
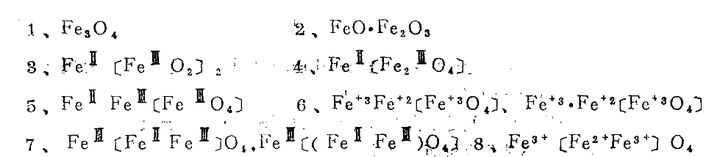
(1)
最简单的化学式写法,只能表达出铁和氧的微粒比,也可以计算出铁的氧化数,但不能说明铁的化合价,更不能说明其结构。
(2)
从这一写法看,把四氧化三铁认为是混合氧化物。但是经过 X 射线证明四氧化三铁中并不存在
和
。
(3)
这一写法把四氧化三铁看成是铁酸亚铁。某些反应似乎证明了这一点,例如:
但 X 射线衍射也证明了四氧化三铁中并不存在铁酸根离子的结构。
(4)
这种写法其实是(3)的另一种形式,同样也因为 X 射线衍射不支持其中含有
而被否定。
(5)
这种写法有一些依据,因为四氧化三铁的确和尖晶石
具有类似的晶体结构,都是立方晶系,而且四氧化三铁每个晶胞容纳 24 个阳离子和 32 个阳离子,相当于 8 个
,亚铁离子和铁离子分布在两种不同的晶格位置上。但是仅仅依靠和尖晶石类似的晶体结构,证据仍然有些不充分
(6)
这个结果是目前经过 X 射线衍射所正式,然后相对被认可程度最高的式子,一般认为其可以代表四氧化三铁的结构。其中包含几个含义:
- 四氧化三铁是一种化合物,而不是混合物。它是一种混合价态的化合物,是复氧化物,而不是盐。其分子中,1 个铁是 +2 价,2 个是 +3 价。
- 四氧化三铁中含有亚铁离子、铁离子和氧离子,是一种离子晶体。
- 四氧化三铁具有反尖晶石结构。
尖晶石是具有实验式 AB2O4 的矿石,其写法一般写成 AB[BO4],代表化合物即尖晶石。其他许多复氧化物,例如 CoAl2O4、ZnFe2O4、Co3O4 等都具有尖晶石结构。尖晶石型晶体结构的 1 个晶胞有 56 个离子,相当于 8 个 AB2O4,其中有 24 个金属离子。尖晶石晶胞结构复杂,简化后可用下图表示:
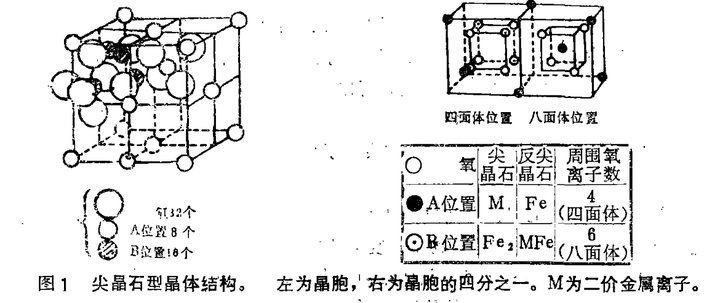
每个晶胞实际上可以分为 8 个小立方体,这 8 个小立方体又可以分为两类。每种各有 4 个。每两个共边的小立方体是同类的,每两个共面的小立方体分属不同类型的结构。
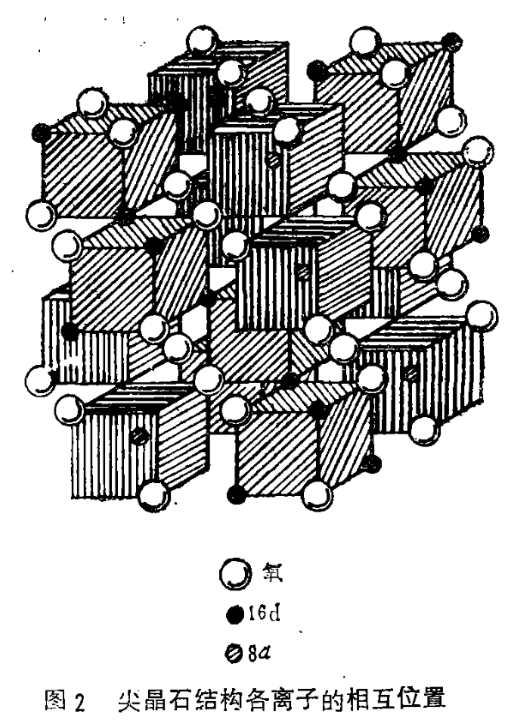
在每个不同类型的小立方体内都有 4 个氧离子,8 个小立方体中,氧离子都位于体对角线中点至顶点的中心。由于氧离子体积而金属离子体积小,因此氧离子为密堆积结构,金属离子填充在氧离子密堆积的空隙中。
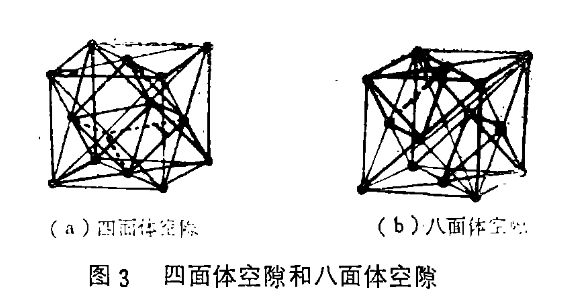
氧离子之间存在 2 种空隙:八面体空隙和四面体空隙。八面体空隙被 6 个氧离子包围而成,空隙较大,也称为 B 位。而四面体空隙由四个氧离子包围而成,空隙较小,也称为 A 位。
尖晶石结构是许多 AB2O4 氧化物中存在的结构,但是仍然有一些符合该组成的氧化物具有另一种反结构,被称为反尖晶石结构。例如 Mg2FeO4,在这个氧化物中,结构中的点阵形式和氧离子分布完全和尖晶石结构一样,但是正离子排布不同,这里不详细展开解释。为了凸显反尖晶石结构和尖晶石结构的不同,具有反尖晶石结构的化合物一般写成 M[MMO4]的形式。例如 Fe3O4、FeCr2O4、MgIn2O4 等。
四氧化三铁的反尖晶石晶体结构中,每个晶胞中有 8 个亚铁离子、16 个铁离子和 32 个氧离子,晶体由氧离子的立方最密堆积构成,铁离子的一半嵌入堆积中四面体的中心位置,而另一半和亚铁离子的全部分布在每个八面体的中心位置,平均下来亚铁离子和铁离子各占一半,因此其结构式写成:
最好,其中 t 表示四面体,o 表示八面体。

